该课题来源于国家自然科学基金面上项目。肿瘤免疫治疗是一种重要的、正在迅速发展的肿瘤治疗新模式。
实体肿瘤主要由肿瘤细胞及肿瘤血管构成,单一抗肿瘤细胞、或单一抗血管生成的免疫治疗效果有限,联合免疫治疗势在必行。
本项目首先研究了脐静脉内皮细胞(HUVEC)疫苗对食管鳞癌的抑制效果。对NOD/SCID小鼠进行免疫重建,发现HUVEC疫苗发挥了明显抑制食管鳞癌生长及抗血管生成效应。但HUVEC是正常的内皮细胞,它与肿瘤血管内皮细胞(TEC)有很大差异,需要对该疫苗进行优化。
采用食管鳞癌细胞培养上清制备的条件培养基诱导HUVEC,发现诱导后HUVEC的迁移、侵袭、小管形成以及Dil-Ac-LDL摄取功能增强,高表达TEC特异性标志(TEM1、TEM8),表明诱导后HUVEC具备TEC特性(称“肿瘤化HUVEC”)。
动物实验证明,与HUVEC疫苗相比,肿瘤化HUVEC疫苗抑制肿瘤生长、抗血管生成能力均明显增强。基因表达谱芯片结果进一步表明,c-Myc在HUVEC向TEC转变过程中起关键作用,JAK/STAT3信号通路参与此过程。二甲双胍可以通过抑制JAK/STAT3/c-Myc信号,从而抑制该转变发挥抗血管生成作用,并在建立的人食管鳞癌PDX模型中证明了二甲双胍的抗血管生成作用。
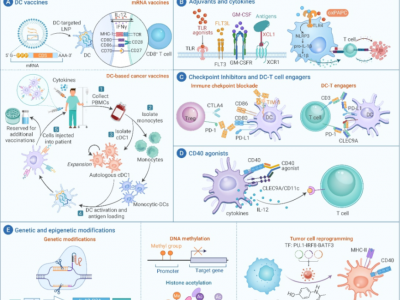
树突状细胞(DC)在体内可激活初始T淋巴细胞,产生CTL杀伤肿瘤细胞。本研究发现负载自身肿瘤组织裂解物的DC反而促进肿瘤血管生成,可能由于肿瘤组织匀浆含有抑制DC功能的细胞因子,诱导其内皮样分化从而促进血管生成。鉴于该方法制备的DC疫苗已有临床应用,此研究结果对其安全性具有警示意义。
基于此,该项目后续研究中抗原的制备采用肿瘤细胞冻融裂解物,离心去除上清中可能抑制DC功能的细胞因子。结果表明该DC疫苗联合肿瘤化HUVEC疫苗对移植瘤的抑制、对肿瘤血管生成的抑制作用均优于单疫苗组。
联合疫苗组小鼠血清中肿瘤血管生成相关抗体水平、脾指数、CTL杀伤效应、IFN-γ水平、脾脏及肿瘤组织中浸润的CD3+CD8+T淋巴细胞数均高于单疫苗组。
该项目采用肿瘤化HUVEC疫苗联合DC疫苗,既杀伤肿瘤细胞,又产生抗肿瘤血管效应,该策略有望成为具有良好应用前景的抗肿瘤免疫治疗新方案。
该项目已发表SCI论文8篇、中文核心期刊论文2篇,已授权发明专利1项、获得科研奖励5项、国际会议报告1次、国际会议壁报1份、培养博士研究生2名、硕士研究生4名、青年教师2名。